På grund av den låga densiteten hos elektronmolnet på pyridinringen är det i allmänhet inte lätt att oxideras, särskilt under sura förhållanden, efter saltet av pyridin har kväveatomen en positiv laddning, och induktionseffekten av elektronabsorption är förstärkt, så att elektronmolndensiteten på ringen blir lägre och oxidationsmedlets stabilitet ökas. När pyridinringen har en sidokedja inträffar sidokedjeoxidationsreaktionen.
Under speciella oxidationsförhållanden kan pyridin genomgå en oxidationsreaktion liknande tertiär amin för att producera N-oxid. Till exempel, när pyridin interagerar med peroxinsyra eller väteperoxid, erhålls pyridin-n-oxid.
Pyridin n-oxid kan reduceras till deoxygenate. I pyridin-n-oxiden kan det odelade elektronparet på syreatomen konjugeras med den aromatiska stora π-bindningen, vilket ökar elektronmolndensiteten på ringen, och ställena och ökar avsevärt, vilket gör pyridinringen till elektrofil substitutionsreaktion lätt att uppstå. På grund av den positiva laddningen på kväveatomen efter genereringen av pyridin n-oxid ökar den inducerade effekten av elektronabsorption, så att elektronmolndensiteten i positionen minskar, så den elektrofila substitutionsreaktionen sker huvudsakligen vid 4( ). Samtidigt är pyridin-n-oxid också benägen för nukleofila substitutionsreaktioner.
I motsats till oxidationsreaktionen är pyridin benägen för hydreringsreduktion av bensenringen, vilket kan reduceras genom katalytisk hydrering och kemiska reagens.
Dec 10, 2023
Lämna ett meddelande
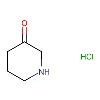
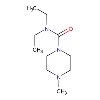
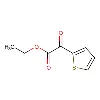
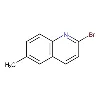
REDOX-reaktion av pyridin
Skicka förfrågan