Kinolin är en heterocyklisk aromatisk organisk förening med ett brett utbud av tillämpningar inom områdena läkemedel, agrokemikalier och materialvetenskap. Som kinolinleverantör blir jag ofta frågad om reaktionsmekanismerna som är involverade i dess syntes. I det här blogginlägget kommer jag att fördjupa de olika reaktionsmekanismerna för kinolinsyntes, vilket ger en omfattande översikt över nyckelprocesserna och deras underliggande principer.
Skraupsyntes
SKRAUP -syntesen är en av de äldsta och mest välkända metoderna för kinolinsyntes. Det rapporterades först av Zdenko Hans Skraup 1880. Reaktionen involverar kondensation av anilin eller ett substituerat anilin med glycerol i närvaro av en stark syrakatalysator, såsom svavelsyra, och ett oxidationsmedel, vanligtvis nitrobensen.
Mekanismen för SKRAUP -syntesen kan delas upp i flera steg. Först är glycerol dehydratiserad i närvaro av den starka syran för att bilda akrolein. Syran protonerar hydroxylgrupperna av glycerol, vilket underlättar eliminering av vattenmolekyler.
Därefter reagerar anilinet med akrolein genom ett Michael -tillägg. Den nukleofila aminogruppen av anilin attackerar den elektrofila ß - kolet av akrolein och bildar en mellanprodukt. Denna mellanprodukt genomgår sedan en intramolekylär cyklisering. Amino -gruppen attackerar karbonylkolet i aldehydgruppen och bildar en cyklisk imin.
Slutligen oxideras den cykliska iminen av nitrobensen för att bilda kinolinringen. Nitrobensen reduceras till anilin under processen. Den övergripande reaktionen är exoterm och kan vara ganska kraftfull, vilket ofta kräver noggrann kontroll av reaktionsbetingelserna.
DOEBNER - Von Miller Synthesis
Doebner - von Miller -syntesen är en annan viktig metod för kinolinsyntes. Det involverar reaktionen av anilin eller en substituerad anilin med en a, p - omättad karbonylförening, såsom crotonaldehyd, i närvaro av en stark syrakatalysator, vanligtvis saltsyra.
Mekanismen för Doebner - von Miller -syntesen börjar med protoneringen av karbonylgruppen för a, ß - omättad karbonylförening. Detta ökar elektrofiliciteten hos p -kolet. Anilinet attackerar sedan p -kolet genom ett michael -tillägg och bildar en mellanprodukt.
Efter tillägget inträffar en intramolekylär cyklisering. Amino -gruppen av anilinet attackerar karbonylkolet och bildar en cyklisk mellanprodukt. Denna mellanprodukt genomgår sedan uttorkning för att bilda kinolinringen. Syrakatalysatorn spelar en avgörande roll för att främja både tillägget och cykliseringsstegen genom att protonera de relevanta funktionella grupperna.
Synteskammar
Kamsyntesen är en metod för framställning av kinoliner från en 1,3 - diketon och en anilin eller ett substituerat anilin i närvaro av en stark syrakatalysator, såsom svavelsyra eller polyfosforsyra.
Reaktionsmekanismen börjar med kondensationen av anilinet med 1,3 - diketon. Amino -gruppen av anilinet attackerar karbonylkolet i en av ketongrupperna i 1,3 - diketon och bildar en imin.
Därefter inträffar en intramolekylär cyklisering. Kväveatomen i iminen attackerar karbonylkolet i den andra ketongruppen i 1,3 - diketon, som bildar en cyklisk mellanprodukt. Denna mellanprodukt genomgår sedan uttorkning för att bilda kinolinringen. Den starka syrakatalysatorn hjälper till att aktivera karbonylgrupperna och främja eliminering av vattenmolekyler.
Pfitzinger reaktion
Pfitzinger -reaktionen används för att syntetisera kinoliner från isatin och en keton eller en aldehyd i närvaro av en stark bas, såsom kaliumhydroxid.
Mekanismen för Pfitzinger -reaktionen börjar med avprotonering av keton eller aldehyd med den starka basen och bildar en enolatjon. Enolatjonen attackerar sedan karbonylkolet i isatin och bildar en mellanprodukt.
Efter tillägget inträffar en ringreaktion. Isatinringen öppnas och en serie omarrangemang äger rum. Slutligen inträffar en cykliseringsreaktion, följt av uttorkning för att bilda kinolinringen. Basen spelar en nyckelroll för att främja bildandet av enolatjonen och underlätta de olika omarrangemangs- och cykliseringsstegen.
Kinoliner
Kinoliner har ett brett utbud av tillämpningar inom läkemedelsindustrin. Många kinolinbaserade föreningar har visat antibakteriella, svampdödande och antimalariala aktiviteter. Till exempel är klorokin ett välkänt antimalariat läkemedel som innehåller en kinolinring.
I den agrokemiska industrin används kinoliner som bekämpningsmedel och herbicider. De kan rikta in sig på specifika enzymer eller receptorer i skadedjur, vilket ger effektiv kontroll av jordbruksskadegörare.
Inom materialvetenskap kan kinoliner användas som byggstenar för syntes av funktionella material, såsom färgämnen och polymerer. Deras aromatiska struktur och elektron - rik natur gör dem lämpliga för olika tillämpningar inom optoelektronik.
Våra kinolinprodukter
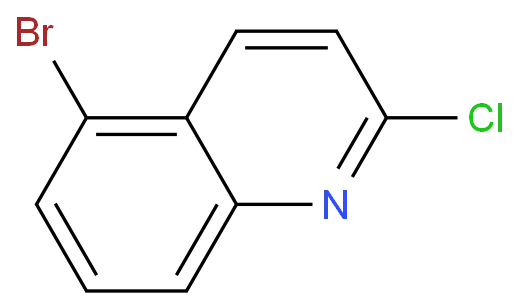
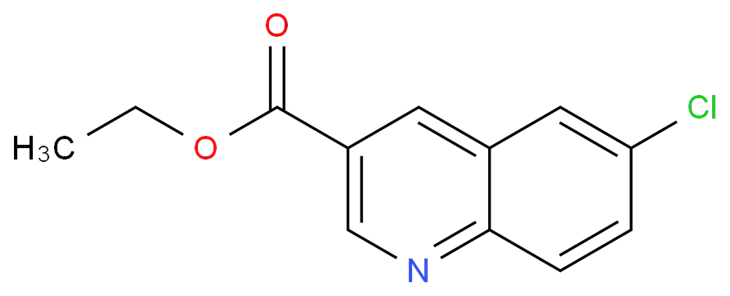
Som kinolinleverantör erbjuder vi ett brett utbud av kinolinsderivat av hög kvalitet. Några av våra populära produkter inkluderar2 - Bromo - 6 - Metylquinolin CAS 302939 - 86 - 2,Etyl 6 - klorokinolin - 3 - karboxylat CAS 375854 - 57 - 2och5 - Bromo - 2 - Chloroquinoline CAS 99455 - 13 - 7. Dessa produkter syntetiseras med tillstånd - av - konstmetoderna och är noggrant kvalitet - kontrollerade för att säkerställa deras renhet och konsistens.
Om du är intresserad av våra kinolinprodukter eller har några frågor om reaktionsmekanismerna för kinolinsyntes, vänligen kontakta oss för ytterligare diskussion och potentiell upphandling. Vi är engagerade i att tillhandahålla de bästa produkterna och tjänsterna för att tillgodose dina behov.
Kontakt för upphandling
Om du är på marknaden för högkvalitativ kinolin och dess derivat, inbjuder vi dig att nå ut till oss för upphandlingsdiskussioner. Oavsett om du är ett läkemedelsföretag, en agrokemisk tillverkare eller en materialvetenskaplig forskare, kan vi tillhandahålla rätt produkter för dina applikationer.
Referenser
- Fieser, LF; Fieser, M. "Advanced Organic Chemistry"; Reinhold Publishing Corporation: New York, 1961.
- Mars, J. "Avancerad organisk kemi: reaktioner, mekanismer och struktur", 4: e upplagan; John Wiley & Sons: New York, 1992.
- Vogel, AI "Textbook of Practical Organic Chemistry", 5: e upplagan; Longman: London, 1989.




